José A. Hernández, Grupo de Biotecnología de Frutales (CEBAS-CSIC)
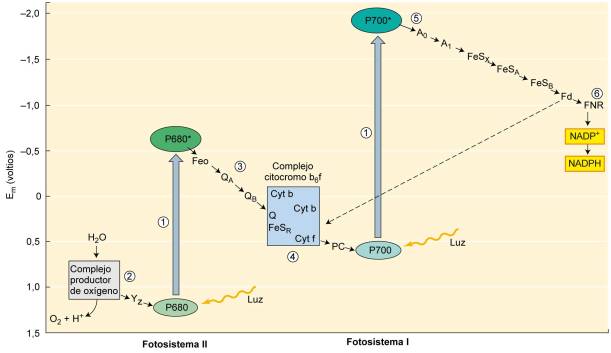
La fluorescencia es un fenómeno foto-físico de las moléculas de clorofila que permite estudiar la función del fotosistema II (PSII) durante el transporte electrónico en la fotosíntesis y la sensibilidad del PSII al daño que puede sufrir por efecto de diferentes estreses, y las consecuencias que esto tiene en el proceso global de la fotosíntesis (Figura 1).
Por tanto, la fluorescencia de clorofilas es una técnica muy útil que permite hacer un seguimiento al proceso de fotosíntesis en general. Se emplea en diferentes estudios:
- Fisiología de la fotosíntesis
- Ecofisiología
- Biología Marina y Acuática
- Horticultura
- Agricultura
- Fisiología de Post-cosecha
- Mejora Vegetal
- Genética
¿Qué es la fluorescencia?
Los electrones que forman parte de un átomo o una molécula tienden a permanecer en un estado de menor energía (estado fundamental). Si un átomo absorbe un fotón con suficiente energía, un electrón puede saltar a un orbital de mayor energía. Este estado de mayor energía es más reactivo que el estado fundamental y puede participar en reacciones químicas que son imposibles para el estado fundamental. Esto es muy importante para la fotosíntesis. Incluso en ausencia de reacciones, el estado excitado es inestable y puede volver a sus estado fundamental por diferentes vías, incluido la emisión de un fotón. El fotón emitido es la fluorescencia.
La energía luminosa absorbida por las moléculas de clorofila en la hoja tiene tres posibles destinos: La mayor parte se va a usar en fotosíntesis (energía fotoquímica). Una pequeña parte de la energía, la que no puede emplearse en fotosíntesis, se disipa en forma de calor o bien puede ser re-emitida como luz (en forma de fluorescencia) con el fin de que el exceso de energía no dañe a los fotosistemas. La cantidad de energía emitida como fluorescencia es muy pequeña (1-2% del total de luz absorbida) (Figura 2).

Figura 2. Esquema mostrando el uso de la energía luminosa en condiciones fisiológicas. La mayor parte se va a usar en fotosíntesis y una pequeña parte de la energía, la que no puede emplearse en fotosíntesis, se disipa en forma de calor o bien puede ser re-emitida como luz (en forma de fluorescencia).
En condiciones normales, la fotosíntesis predomina sobre los otros procesos, pero en condiciones de estrés, la planta no puede trabajar a pleno rendimiento y el exceso de energía debe disiparse. Como consecuencia, los procesos no fotoquímicos aumentan.
Para un análisis de fluorescencia es conveniente adaptar a la planta a condiciones de oscuridad durante unos 10-15 minutos. Cuando una hoja se transfiere desde la oscuridad a la luz, los centros de reacción del PSII se van cerrando progresivamente. Esto da lugar a un aumento en el rendimiento de la fluorescencia de las clorofilas. A partir de este momento, los niveles de fluorescencia disminuyen de nuevo. Este fenómeno se conoce como quenching y se explica de dos maneras: Primero, se produce un incremento en la tasa de transporte de electrones fuera del PSII. Esto es debido a la activación mediada por luz de los enzimas implicados en el metabolismo del carbono y en la apertura de los estomas. Este tipo de quenching se denomina “quenching fotoquímico”. Al mismo tiempo, se produce un aumento de la eficiencia en la que la energía se convierte en calor. Este último proceso se denomina “quenching no fotoquímico” (NPQ).
Para el análisis de la fluorescencia de clorofilas se han definido y calculado diferentes coeficientes para cuantificar el quenching fotoquímico y no fotoquímico. Para los procesos fotoquímicos, el parámetro más útil para medir la eficiencia del PSII es el rendimiento cuántico del PSII (ØPSII o Y(II)), que mide la proporción de luz absorbida por la clorofila asociada al PSII que es usada en procesos fotoquímicos. Otro parámetro ampliamente usado es el quenching fotoquímico (qP). Aunque es muy similar al ØPSII , el significado del qP es algo diferente. En este caso, el qP hace referencia a la proporción de centros de reacción del PSII que están abiertos. ØPSII y qP están interrelacionados con un tercer parámetro, Fv/Fm, que mide la eficiencia del PSII, es decir, mide el rendimiento cuántico si todos los centros de reacción del PSII estuviesen abiertos.
Los procesos no fotoquímicos (NPQ) están relacionados con la disipación de calor, y su escala varía desde 0 hasta el infinito. El NPQ tiene varios componentes, pero el más importante es el denominado qN (coeficiente del quenching no fotoquímico). Este parámetro varía en una escala desde 0 a 1 y está relacionado con la disipación de calor mediante el ciclo de las xantofilas (Fig 3). NPQ y qN son indicadores de estrés y han demostrado ser parámetros muy sensibles para la detección temprana de condiciones de estrés mediante imagen de fluorescencia. En este sentido se pueden usar para valorar situaciones de estrés abiótico como biótico, pudiendo analizar el efecto de estreses ambientales en el cloroplasto, incluso antes de que se observen señales de síntomas en las hojas (Fig 4).

Figura 3. Esquema del ciclo de las Xantofilas. La interconversión de anteroxantina en zeaxantina lleva asociada una disipación de energía en forma de calor.

Figura 4. Efecto del estrés hídrico sobre los parámetros qP y qN. Las plantas 1,2 y 3 se sometieron a un periodo de falta de riego de 15 días. Las imágenes muestran cómo el estrés reduce el valor de qP, pero de forma más dramática en plantas 1 y 2. Por el contrario, la sequía aumenta la disipación de calor (qN) en las plantas 1 y 2 con el fin de poder minimizar daños por exceso de energía luminosa. La planta 3 presenta sólo una pequeña variación en qN.
Para más información:
- Maxwell K, Johnson GN (2000) Chlorophyll fluorescence – a practical guide. J. Exp. Bot. 51: 659-668.
- Pérez-Bueno ML, Ciscato M, vandeVen M, Gacía-Luque I, Valcke R, Barón M (2006) Imaging viral infection: studies on Nicotiana benthamiana plants infected with the pepper mild mottle tobamovirus. Photosyntesis Research 90:111–123.
- Taiz L, Zeiger E (2010) Plant Physiology, Fifth Edition, Sinauer Associates Inc., Publishers, Sinderland, Massachusetts, USA